こんにちは。
認知症の新薬として登場したレカネマブ(LEQEMBI)。
以前、登場したアドゥカマヌブは問題があったとして認可を取り消されましたが、今回は大丈夫なのでしょうか。
●レカネマブとは
出典:https://medical.jiji.com/news/57002
レカネマブとはアドゥカマヌブ同様に日本のエーザイと米バイオジェンが共同開発した認知症に対する薬。
アデュカヌマブが水に溶けない形のアミロイドβにより強く結合するのに対し、レカネマブは、神経細胞に対する毒性がより強いと考えられている「プロトフィブリル」と呼ばれる、水に溶ける形のアミロイドβを標的としているそうです。
従来の薬では神経細胞に作用し、伝達を活発にして症状の一時的な改善を図っていましたが、レカネマブは異常なたんぱく質を取り除いて早期の認知症進行を緩やかにします。
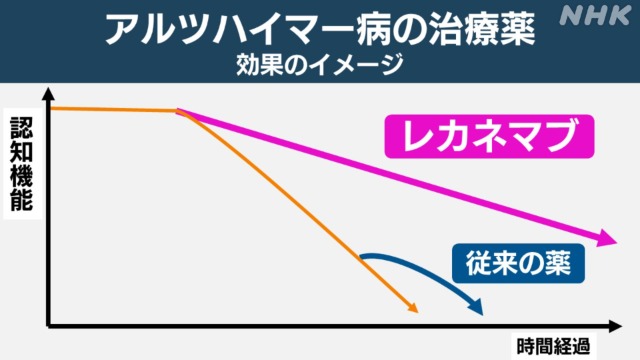
出典:https://www.nhk.or.jp/shutoken/newsup/20220929b.html
アメリカ食品医薬品局(FDA)に迅速承認された後、2023年1月に発表された臨床試験では「治験開始から18カ月後に患者の認知機能を評価したところ、レカネマブを投与された患者では、プラセボ(偽薬)を投与された患者に比べ、認知機能の低下が27%少なかった」とされました。
FDAは「アルツハイマー病の根本を標的にした薬として初めて有用性を示した」と評価しています。
一方、副作用は頭痛や脳の一時的な腫れがあり、特に抗凝固薬を服用中の人は脳出血のリスクが高まるため注意が必要とされています。
では、アドゥカマヌブのように承認取り消しとなる可能性はあるのでしょうか?
●アドゥカマヌブとの違い
アドゥカマヌブは条件付き承認後、以下の3点から承認が取り消されました。
①二つの試験の結果に一貫性がない
1回目のデータと2回目のデータに差異がある。
②アミロイドβ低下と症状の進行抑制との関連が不明確
アミロイドβ減少と認知機能低下予防の相関性が示せていない。
③投与により脳の浮腫や微小出血などがみられる
治験を受けたグループの約35%に浮腫、約19%に微小出血を認めた。
今回はデータ面で前よりしっかりと出ており、アドゥカマヌブと同じアミロイドβではなく、プロトフィブリルと呼ばれる水溶性のアミロイドβに作用しています。
また、脳浮腫などデメリットはありますが、アドゥカマヌブがデメリットの方が多い気意図された一方、レカネマブはメリットの方が大きいとされました。
現状、レカネマブはこのまま臨床現場に出てくるかもしれません。
●今後のリハビリは?
では、リハビリはどう変わるかですが、あまり変わらないかもしれません。
今回レカネマブが効果を出しているのは早期の認知症。
まだリハビリが関わらないことも多い時期です。
ですが、地域のサロンなどに行く場合は早期の方もいる可能性があり、レカネマブとサロンの併用もあるかもしれません。
コグニサイズとレカネマブの合わせ技もあるかもしれませんね。
いかがだったでしょうか?
日本では2023年秋以降に承認される可能性があるとのことで、現場で見ることも近いかもしれません。
認知症の新薬として希望の光となってくれることを切に願います。
アドゥカマヌブの詳細はこちら。
それではまた次回の記事でお会いしましょう。